А. Опыты Резерфорда
В 1911 г. Резерфорд провел исключительные по своему значению эксперименты, доказавшие существование ядра атома. Для исследования атома Резерфорд применил его зондирование (бомбардировку) с помощью α-частиц, которые возникают при распаде радия, полония и некоторых других элементов. Резерфордом и его сотрудниками еще в более ранних опытах в 1909 г. было установлено, что α-частицы обладают положительным зарядом, равным по модулю удвоенному заряду электрона q =+2e, и массой, совпадающей c массой атома гелия, то есть
Однако дочерняя сторона химического разделения предназначена только для распада, поскольку нет средств для пополнения запаса преобразованных атомов. Резерфорд и Содди видели, что, по-видимому, постоянная деятельность урана, тория и радия связана с периодами полураспада, которые по сравнению с человеческими жизнями являются длинными. Это понимание преодолело головоломку в основе всех предыдущих теорий; ибо если бы полная радиоактивность во Вселенной становилась все меньше и стремилась исчезнуть, закон сохранения энергии не нарушался бы.
m а = 6,62 · 10 -27 кг,
что примерно в 7300 раз больше массы электрона. Позже было установлено, что α-частицы представляют собой ядра атомов гелия. Этими частицами Резерфорд бомбардировал атомы тяжелых элементов. Электроны вследствие своей малой массы не могут изменить траекторию α-частαицы. Их рассеяние (изменение направления движения) может вызвать только положительно заряженная часть атома. Таким образом, по рассеянию α-частиц можно определить характер распределения положительного заряда, а значит, и массы внутри атома.
Они считают радиоактивность фундаментальным свойством природы, подходящим для присоединения к избранной группе электричества, магнетизма, света и силы тяжести. Не менее примечательная вещь в этой теории, которая провозглашала, что атом не был нерушимым, был бесспорным способом, в котором он был принят. Помимо пожилого и неизменного Лорд Келвин и постоянно спорного Генри Армстронг, теория трансформации встречается мало оппозиция, химики, особенно, хотя он нарушает представления о неизменности атомов, что они «всасываются с молоком матери», не может опровергнуть доказательств и в лучшем случае мог бы принять ожидаемое отношение.
Было известно, что α-частицы, излученные полонием, летят со скоростью 1,6-107 м/с. Полоний помещался внутрь свинцового футляра, вдоль которого высверлен узкий канал. Пучок α-частиц, пройдя канал и диафрагму, падал на фольгу. Золотую фольгу можно сделать исключительно тонкой – толщиной 4-10 -7 м (в 400 атомов золота; это число можно оценить, зная массу, плотность и молярную массу золота). После фольги α-частицы попадали на полупрозрачный экран, покрытый сульфидом цинка. Столкновение каждой частицы с экраном сопровождалось вспышкой света (сцинтилляцией), обусловленной флуресценцией, которая наблюдалась в микроскоп.
В большой степени Резерфорд провел следующие годы, разворачивая эту богатую жилу интерпретации. Работая с Содди и используя новую машину для жидкого воздуха, предоставленную Макгиллом своим богатым благодетелем, он конденсировал эманацию при низких температурах, доказывая, что это газ. Другие тесты убедили их, что эманация принадлежит к семейству инертных газов, обнаруженных незадолго до этого сэром Уильямом Рамсей. Такая работа была очень важна, поскольку было множество радиоэлементов, из которых химическая идентичность и место в серии распада были неопределенными.
При хорошем вакууме внутри прибора (чтобы не было рассеяния частиц от молекул воздуха) в отсутствие фольги на экране возникал светлый кружок из сцинтилляций, вызываемых тонким пучком α-частиц. Когда на пути пучка помещалась фольга, то подавляющее большинство α-частиц все равно не отклонялось от своего первоначального направления, то есть проходило сквозь фольгу, как если бы она представляла собой пустое пространство. Однако имелись α-частицы, которые изменяли свой путь и даже отскакивали назад.
В чем логическая непоследовательность планетарной модели атома?
Особый интерес вызвал гелий, хотя и не являющийся радиоэлементом, из-за уверенности Резерфорда в том, что в качестве положительного иона он был идентичен альфа-частице. И альфа-частица, имеющая весомую массу, он считал ключом в переходе от элемента одного атомного веса к элементу другого. Он очаровывал Резерфорда и потому, что он мог оценить огромную скорость и энергию, с которыми он был выброшен из разлагающегося атома.
Поскольку Болтвуд оставался в Нью-Хейвене, штат Коннектикут, его сотрудничество с Резерфордом проводилось по почте. Эта работа была продолжена от определения количества радия, присутствующего на грамм урана в минералах, к предложению Резерфорда о том, что если бы количество и скорость образования конечного продукта серии были известны, можно было бы вычислить возраст минерала. Струтт в Англии следовал этой идее, используя гелий, обнаруженный в радиоактивных веществах; но переменное количество этого газа, которое удалось избежать, допускало только минимальное определение возраста.
Марсден и Гейгер, ученики и сотрудники Резерфорда, насчитали более миллиона сцинтилляций и определили, что примерно одна из 2 тысяч α-частиц отклонялась на углы, большие 90°, а одна из 8 тысяч – на 180°. Объяснить этот результат на основе других моделей атома, в частности Томсона, было нельзя.
Расчеты показывают, что при распределении по всему атому положительный заряд (даже без учета электронов) не может создать достаточно интенсивное электрическое поле, способное отбросить α-части-цу назад. Напряженность электрического поля равномерно заряженного шара максимальна на поверхности шара и убывает до нуля по мере приближения к центру. Рассеяние α-частиц на большие углы происходит так, как если бы весь положительный заряд атома был сосредоточен в его ядре – области, занимающей весьма малый объем по сравнению со всем объемом атома.
Болт-дерево показало универсальное появление свинца с урановыми минералами; считал это конечным продуктом серии; и, используя значение Резерфорда для периода полураспада радия и их величину для количества радия в графе урана, смог рассчитать скорость образования свинца. Возраст некоторых из его образцов горных пород составлял более миллиарда лет, впервые давая количественное доказательство древности Земли.
Многие другие проблемы в области радиоактивности проводились Резерфордом, иногда в одиночку, иногда с одним из студентов-исследователей в сильной школе, которую он создал. Среди проектов в его лаборатории были измерения энергии излучения, исследования свойств бета - и гамма-лучей, попытки изменения скоростей затухания в экстремальных условиях температуры, попытки размещения актиния в серии распада и исследования радиоактивности земли и атмосферы.
Вероятность попадания α-частиц в ядро и их отклонение на большие углы очень мала, поэтому для большинства α-частиц фольги как бы не существовало.
Резерфорд теоретически рассмотрел задачу о рассеянии α-частиц в кулоновском электрическом поле ядра и получил формулу, позволяющую по плотности потока α-частиц, налетающих на ядро, и измеренному числу частиц, рассеянных под некоторым углом, определить число N элементарных положительных зарядов +е, содержащихся в ядре атомов данной рассеивающей фольги. Опыты показали, что число N равно порядковому номеру элемента в периодической системе Д. И. Менделеева, то есть N = Z (для золота Z = 79).
Он пользовался большим спросом в качестве оратора и часто ездил в отдаленные районы Соединенных Штатов и Англии, выступал с лекцией, серией переговоров или курсом летней сессии. Хотя от него нельзя было отказываться от чести выступать в Королевском институте, в лекции Бейкера по королевскому обществу или в лекциях Силлимана в Йельском университете, некоторые доброжелатели призывали его ограничить свои внешние обязательства. Его время также использовалось в письменной форме «Радио-активность», первый учебник по этому предмету и признанный классиком при его публикации.
Таким образом, гипотеза Резерфорда о сосредоточении положительного заряда в ядре атома позволила установить физический смысл порядкового номера элемента в периодической системе элементов. В нейтральном атоме должно содержаться также Z электронов. Существенно, что число электронов в атоме, определенное различными методами, совпало с числом элементарных положительных зарядов в ядре. Это послужило проверкой справедливости ядерной модели атома.
Так быстро развился прогресс науки, однако, что Резерфорд подготовил второе издание в следующем году, которое было на 50 процентов больше. Как только это было сделано, он столкнулся с задачей создания лекций Силлимана в книге. Неудивительно, что он ограничил свое письмо журналами в течение следующих нескольких лет.
Настоящие осадки почестей начали спускаться на него, продолжая всю оставшуюся жизнь. Резерфорд полностью наслаждался этим признанием, потому что, хотя и не напрасно, он полностью осознавал свою собственную ценность. Пока он был счастлив в Макгилле, Резерфорд хотел вернуться в Англию, где он был бы ближе к ведущим научным центрам мира.
Б. Ядерная модель атома Резерфорда
Обобщая результаты опытов по рассеянию α-частиц золотой фольгой, Резерфорд установил:
♦ атомы по своей природе в значительной мере прозрачны для α-частиц;
♦ отклонения α-частиц на большие углы возможны только в том случае, если внутри атома имеется очень сильное электрическое поле, создаваемое положительным зарядом, связанным с большой и сконцентрированной в очень малом объеме массой.
Резерфорда привлекла в Манчестер необычайно талантливую группу студентов-исследователей, которые внесли глубокий вклад в физику и химию. По возвращении в Англию в Резерфорде было всего несколько миллиграммов радиоактивных материалов, что было недостаточно для его собственных исследований. В великодушном жесте Австрийская академия наук отправила из контролируемых им урановых рудников Йоахимсталь около 350 миллиграммов хлорида радия в качестве совместного займа Резерфорду и Рамсей. К сожалению, Рамсей хотел сохранить свое владение на неопределенный срок, в то время как оба увидели мудрость оставить предложение безраздельным: до тех пор, пока венские власти не отправили еще один сопоставимый источник радиума для эксклюзивного использования Резерфорда, он был ограничен работой с «ничьей» эманации, которую Рамсей послал периодически из Лондона.
Для объяснения этих опытов Резерфорд предложил ядерную модель атома: в ядре атома (области с линейными размерами 10 -15 -10 -14 м) сосредоточены весь его положительный заряд и практически вся масса атома (99,9 %). Вокруг ядра в области с линейными размерами ~10 -10 м (размеры атома оценены в молекулярно-кинетической теории) движутся по замкнутым орбитам отрицательно заряженные электроны, масса которых составляет лишь 0,1 % массы ядра. Следовательно, электроны находятся от ядра на расстоянии от 10 000 до 100 000 поперечников ядра, то есть основную часть атома составляет пустое пространство.
Сформулируйте основной результат опыта Резерфорда
В определенной степени это определило большинство первоначальных исследований Резерфорда в Манчестере, обширное исследование эманации радия: но он всегда находил эманацию и ее активные продукты распада месторождения более удобными источниками, чем сам радий.
Эманацию можно было легко очистить в жидком воздухе, и Резерфорд вскоре определил объем этого газа в равновесии с одним грамом радия. Камерона и, подтвердив его расчетную величину, устранили некоторые сомнения в отношении точности радиоактивных данных и теории. С помощью спектроскопа-копира Томаса Ройдса Резерфорд затем сфотографировал спектр эманации, не исследованный, так как визуальные наблюдения Рамзая и Колли в этой работе включали его в научные споры, которые он обычно стремился избежать; но после того, как Содди покинул лабораторию Рамсей, вклад последнего в радиоактивность был отмечен за их почти единообразную неправильность.
Ядерная модель атомов Резерфорда напоминает солнечную систему: в центре системы находится «солнце» – ядро, а вокруг него по орбитам движутся «планеты» – электроны, поэтому данную модель называют планетарной. Электроны не падают на ядро потому, что электрические силы притяжения между ядром и электронами уравновешиваются центробежными силами, обусловленными вращением электронов вокруг ядра.
Хотя эксперт по обработке небольших количеств редких газов, Рамсей никогда не брал на себя труд, чтобы хорошо изучить методы радиоактивности. Его неточная работа в сочетании с сильным желанием получить приоритет привела его к быстрому опубликованию многочисленных результатов, которые Резерфорд и другие в этой области были вынуждены исправить. Никогда не ограничивать рамки своих исследований - он предпочитал продвигаться по радиоактивности по широкому пути - Рутерфорд преследовал «свои» альфа-частицы.
В них были его фавориты: бета-частицы были слишком малы и, будучи электронами, слишком распространены. Альфы, однако, были массивными, с атомным размером: и он мог четко представить себе, как они выходят из своих родительских атомов с огромной скоростью и энергией. Конечно, это будет ключом к классической цели физика: понимание природы материи. До тех пор ничто не изменило раннего убеждения Резерфорда, что альфа-частица была двузарядным атомом гелия, но ему не удалось доказать эту веру. Ионизация при столкновении, процесс, изученный бывшим коллегой Резерфорда в Кембридже, Дж.
В 1914 г., через три года после создания планетарной модели атома, Резерфорд исследовал положительные заряды в ядре. Бомбардируя электронами атомы водорода, он обнаружил, что нейтральные атомы превратились в положительно заряженные частицы. Так как атом водорода имеет один электрон, Резерфорд решил, что ядро атома является частицей, несущей элементарный положительный заряд +е. Эту частицу он назвал протоном.
Таунсендом, вызвал увеличение заряда одной частицы, достаточное для того, чтобы дать электрометру измеримый «удар». Таким образом, они смогли подсчитать в первый раз точно и прямо, количество альфа-частиц, испускаемых в секунду из грамма радия. Этот эксперимент позволил Резерфорду и Гейгеру подтвердить, что каждая альфа-частица вызывает слабую, но дискретную вспышку, когда она ударяет по люминесцентному экрану сульфида цинка и, следовательно, непосредственно ведет к широко распространенному методу сцинтилляционного счета.
Это было также источником электрических и электронных методов подсчета частиц, в которых позднее был основан Гейгер. Но в это время сцинтилляционная техника, которая теперь оказалась надежной, была более удобной. Они измерили общий заряд из источника радия и разделили его на количество альфа, подсчитанное для получения заряда на частицу. Но Резерфорд все же желал решительных, прямых доказательств; и здесь ему помог его опытный стеклодув.
Планетарная модель хорошо согласуется с опытами по рассеиванию α-частиц, но она не может объяснить устойчивость атома. Рассмотрим, например, модель атома водорода, содержащего ядро-протон и один электрон, который движется со скоростью v вокруг ядра по круговой орбите радиуса r. Электрон должен по спирали падать на ядро, и частота его обращения вокруг ядра (следовательно, и частота излучаемых им электромагнитных волн) должна непрерывно изменяться, то есть атом неустойчив, и его электромагнитное излучение должно иметь непрерывный спектр.
Такую трубку заполняли эманацией и помещали в большую трубку из более толстого стекла. Со временем альфа-частицы от распадающейся эманации проникли внутрь и были заперты в пространстве между внутренними и внешними трубами: когда Ройдс зажег материал в этом пространстве, они увидели спектр гелия. Как и в Монреале, Резерфорд нашел химическую помощь в Манчестере самого высокого качества. Болтвуд провел с ним год, в течение которого они более точно определяли скорость производства гелия радием. Объединив эти результаты с результатами упомянутых выше опытов подсчета, они получили число Авогадро больше, чем когда-либо прежде.
В действительности оказывается, что:
а) атом устойчив;
б) атом излучает энергию лишь при определенных условиях;
в) излучение атома имеет линейчатый спектр, определяемый его строением.
Таким образом, применение классической электродинамики к планетарной модели атома привело к полному противоречию с экспериментальными фактами. Преодоление возникших трудностей потребовало создания качественно новой – квантовой – теории атома. Однако, несмотря на свою несостоятельность, планетарная модель и сейчас принята в качестве приближенной и упрощенной картины атома.
В периодическую таблицу были также новые исследователи - Александр Рассел, Казимир Фаянс и Георг фон Хевези, создающие информацию и идеи, на основе которых были бы установлены законы смещения и концепция изотопии, а также работа над разветвлением серии распада, периодами короткоживущих элементов и других радиохимических проблем.
Величайшее открытие Резерфорда в Манчестере - по сути, его карьеры - было ядерной структурой атома. В ретроспективе его происхождение можно увидеть в незначительных свидетельствах рассеяния альфа-частиц в тонких металлических фольгах или листах слюды, которые он заметил в то время как в Макгилле, и в аналогичном рассеянии молекулами воздуха в своих более поздних экспериментах по электрическому счету с Гейгером. Для того, чтобы больше узнать об этом рассеянии, как из-за того, что он вводил экспериментальные трудности, приводящие к менее точным результатам, так и потому, что он был связан с озадачивающим вопросом о характере поглощения альфа-и бета в материи, Гейгер сделал количественное исследование этого явления.
МИНИСТЕРСТВО ВЫСШЕГО И СРЕДНЕГО СПЕЦИАЛЬНОГО ОБРАЗОВАНИЯ РФ.
НОВОСИБИРСКИЙ ГОСУДАРСТВЕННЫЙ АРХИТЕКТУРНО-СТРОИТЕЛЬНЫЙ УНИВЕРСИТЕТ
кафедра физики
РЕФЕРАТ
Опыты Резерфорда
Выполнил: Кузнецов И.А. (группа 226)
Проверил: Берхоер Л.Д.
Новосибирск 2000 г.
Эрнест Резерфорд – один из самых знаменитых физиков первой половины XX века. Когда-то Резерфорд первый анатомировал атом, обнаружив в нем ядро. Он исследовал сложные явления, протекающие в этой поразительно малой частице вещества, а затем в своей лаборатории расщепил ядра атомов.
Еще будучи студентом 2-го курса университета Резерфорд на одной из конференций выступил с докладом на тему «Эволюция элементов». Резерфорд высказал предположение, что все химические элементы представляют собой сложные химические системы, состоящие из одних и тех же элементарных частиц. В то время атом считался неделимым – в физике господствовала теория Дальтона о неделимости атомов.
Первая попытка создания на основе накопленных экспериментальных данных модели атома принадлежит ДЖ. ДЖ. Томсону. Электроны, как думал Томсон, вкраплены в сверхминиатюрную сферу диаметром 10 –8 см., в которой равномерно распределены положительные заряды. Вместе с отрицательно заряженными электронами сфера электрически нейтральна. Это и есть атом. В то время так думал и Резерфорд, работавший в одной лаборатории с Томсоном, и даже не мечтал, что сможет создать более совершенную модель, основанную на новых представлениях.
В 1896 г, изучая люминесценцию различных веществ, А.Беккерель случайно обнаружил, что соли урана излучают без предварительного их освещения. Это излучение обладает большой проникающей силой и способно воздействовать на фотографическую пластинку, завернутую в черную бумагу. Резерфорд тотчас занялся изучением Беккерелиевых лучей. Он начал исследования рентгеновских лучей с проверки своего предположения о связи между рентгеновскими и беккерелиевыми лучами. Эта мысль пришла к нему в голову по очень простой причине: и те и другие производили ионизацию воздуха. Эта идея не увенчалась успехом.
Но наиболее важным результатом Резерфорда было открытие;-частиц в составе излучения, испускаемого ураном. Резерфорд поместил урановый источник в сильное магнитное поле и разделил излучение на три различных его вида. Иными словами, он открыл тогда состав радиоактивности: альфа– и бета–частицы и гамма-лучи.
Получив;-частицы, Резерфорд тотчас же сделал гениальное заключение, что именно они представляют собой мощный инструмент для проникновения в глубь атома. Как подтвердилось позднее, это было абсолютно правильно. В последующих работах Резерфорд широко использовал;-астицы в качестве снарядов, проникающих в сердце атома – атомное ядро.
Резерфорд открыл эманацию тория и доказал, что этот радиоактивный газ, выделяющийся из тория, представляет собой химический элемент, отличающийся от самого тория. Позднее он определил атомный вес эманации и показал, что она представляет собой благородный газ нулевой группы системы Д.И.Менделева.
Резерфорд и Фредерик Содди впервые объясняют радиоактивный распад как самопроизвольный переход одних элементов в другие. После эманации тория Резерфорд открыл эманацию радия – радон. Ученому было ясно, что радий, испуская;-частицы, превращается в новое активное вещество, подобно эманации тория. Это открытие окончательно подтверждало теорию радиоактивного распада.
В начале 1903 года Резерфорд опытным путем пытается определить химический состав;-частиц. Идея заключается в том, чтобы сравнить массу;-частицы с массами атомов известных элементов. Опыт позволил ему первому идентифицировать;-частицы с атомами гелия. Позднее это подтвердилось и спектрографически.
В 1908 году Резерфорд приступил к широким опытам по исследованию;-частиц методом подсчета их с помощью сцинтилляционного счетчика Гейгера.
![]() Вместе с Гейгером и Ройдсом Резерфорд произвел серию опытов, подтверждавших, что;-частицы есть ничто иное как дважды ионизированные (т.е. потерявшие по 2 электрона) атомы гелия. Этот исторический опыт, благодаря которому уже ни у кого не могло остаться сомнения в правильности его теории распада, заключался в следующем:
Вместе с Гейгером и Ройдсом Резерфорд произвел серию опытов, подтверждавших, что;-частицы есть ничто иное как дважды ионизированные (т.е. потерявшие по 2 электрона) атомы гелия. Этот исторический опыт, благодаря которому уже ни у кого не могло остаться сомнения в правильности его теории распада, заключался в следующем:
в запаянную трубку 2 Резерфорд поместил некоторое количество радона – эманации радия. Толщина стенок этой трубки 0,01 мм. Они достаточно тонки, чтобы испускаемые радоном;-частицы могли проходить через них во внешнюю трубку 3. Перед опытом трубка 3 тщательно откачивалась, и в ней спектрографическим путем нельзя было обнаружить линий гелия. Через несколько дней в трубке 3 обнаружилось накопление газа. Повышая давление в приборе, накопившийся газ можно было сконцентрировать в трубке 1. Через трубку пропускался электрический заряд и тогда оказывалось, что в ней спектральный анализ показывает характерные линии гелия. В трубке был гелий. Но может быть он попал в трубку 2 по недосмотру вместе с радоном, а оттуда проник в трубки 3 и 1? Контрольный опыт дал на этот вопрос отрицательный ответ. Точно в такой же прибор (в трубку 2) Резерфорд помещал не радон, а чистый гелий. Однако через несколько дней в трубке 1 линии гелия не обнаруживались. Гелий не мог пройти через стеклянные стенки трубки 2 в трубку 3. ;-частицы же легко проходили через стекло и накапливались в трубке 3, а затем концентрировались в трубке 1, где и подвергались спектральному анализу, давая линии гелия.
После этого Резерфорд, вместе с Гейгером и Марсденом провели новую серию экспериментов. Результаты произвели переворот в физике. Это была наиболее драматическая глава в науке нашего времени. Резерфорд открыл атомное ядро и тем самым основал новую исключительно важную науку – ядерную физику.
Что это были за эксперименты? Резерфорд и Гейгер на первых порах продолжили наблюдения сцинтилляций, вызываемых;-частицами при ударе о люминесцентный экран из сернистого цинка. Прежде всего опыты привели Резерфорда к заключению, что каждая вспышка (сцинтилляция) вызывается одной;-частицей. Таким образом оправдалось предположение, выдвинутое им ранее. Резерфорд писал тогда, что наблюдение сцинтилляций на экране из сернистого цинка представляет собой очень удобный способ счета частиц, если каждая частица вызывает вспышку. Следовательно, если каждая вспышка вызвана одной;-частицей, то перед физиками открывается возможность наблюдать за поведением отдельных атомов.
Резерфорд и Гейгер визуально подсчитали, что в продолжение секунды из излучателя в одну тысячную грамма радия вылетает 130 000 ;-частиц. Точность подсчета была безукоризненна. Оба ученых, к которым позднее присоединился Марсден, помногу часов проводили в затемненной лаборатории за утомительным счетом сцинтилляций. Гейгер рассказывал, что ему одному пришлось подсчитать в общей сложности миллион;-частиц.
Свою работу начал ученик Резерфорда Марсден. Ему было поручено считать;-частицы, проходящие через тонкие металлические пластинки. Эти пластинки помещались в прибор между излучателем;-частиц и люминесцентным экраном.
Поручая Марсдену эту работу, Резерфорд не рассчитывал обнаружить что=либо любопытное. При условии, что модель атома Томсона правильна (а тогда не было никаких причин сомневаться в этом), опыт должен был показать, что;-частицы свободно проходят через металлические преграды. Однако что-то все-таки заставило Резерфорда пойти на этот новый эксперимент.
Марсдена поразило, что;-частицы в этом простом опыте ведут себя иначе, чем должны вести, если принять модель атома такой, какой ее предложил Томсон. Согласно модели Томсона положительный заряд распределен по всему объему атома и уравновешивается отрицательным зарядом электронов, каждый из которых имеет массу гораздо меньшую, чем масса;-частицы. Поэтому даже в редких случаях, когда;-частица столкнется с гораздо более легким по сравнению с ней электроном, она может лишь незначительно отклониться от своего прямолинейного пути. Но в опытах Марсдена;-частицы отнюдь не беспрепятственно проходили через металлическую пластинку. Нет, некоторые из них отклонялись после удара о пластинку на угол около 150 о, т.е. почти обратно возвращались к излучателю. Таких возвращавшихся частиц было, правда, очень мало. Когда экспериментатор преграждал путь;-частицам более толстой пластинкой, то в его поле зрения появлялось больше;-частиц, отклонившихся на большие углы. Это указывало, что замеченное Марсденом рассеяние;-частиц не представляет собой какого-то поверхностного эффекта, т.е. оно не связано с поверхностью пластинки. Но Марсден не мог высказать каких-либо соображений по поводу увиденного им странного поведения;-частиц. Он рассказал подробно о своих наблюдениях Резерфорду.
Позднее Резерфорд признался, что сообщение Марсдена произвело на него потрясающее впечатление: «это было почти неправдоподобно, как если бы вы выстрелили пятнадцатифунтовым снарядом в кусок папиросной бумаги и снаряд отскочил бы обратно и поразил вас».
Резерфорд сразу представил себе, что эффект, наблюдаемый Марсденом, мог быть только в одном случае: если;-частица, проникнув в атом, натыкалась на какую-нибудь массивную преграду, имеющуюся в нем, и отбрасывалась, получив при столкновении мощный удар.
На основании этих исследований Резерфорд предположил ядерную (планетарную) модель атома. Согласно этой модели, вокруг положительного ядра, имеющего заряд ze (z – порядковый номер элемента в системе Менделеева, e – элементарный заряд), размер 10 -15 – 10 -14 м и массу, практически равную массе атома, в области с линейными размерами порядка 10 -10 м по замкнутым орбитам движутся электроны, образуя электронную оболочку атома. Так как атомы нейтральны, то заряд ядра равен суммарному заряду электронов, т.е. вокруг ядра должно вращаться z электронов.
Для простоты предположим, что электрон движется вокруг ядра по круговой орбите радиуса r. При этом кулоновская сила взаимодействия между электроном и ядром сообщает электрону центростремительное ускорение. Второй закон Ньютона для электрона, движущегося по окружности под действием кулоновской силы, имеет вид ![]() , где m e
и v – масса и скорость электрона на орбите радиуса r, - электрическая постоянная.
, где m e
и v – масса и скорость электрона на орбите радиуса r, - электрическая постоянная.
Данное уравнение содержит два неизвестных: r и v. Следовательно, существует бесчисленное множество значений радиуса и соответствующих ему значений скорости (а значит и энергии), удовлетворяющих этому уравнению. Поэтому величины r, v (следовательно и E) могут меняться непрерывно, т.е. может испускаться любая, а не вполне определенная порция энергии. Тогда спектры атомов должны быть сплошными. В действительности же опыт показывает, что атомы имеют линейчатый спектр. Также из данного выражения следует, что при м скорость движения электронов м/с, а ускорение м/с 2 . Согласно классической электродинамике, ускоренно движущиеся электроны должны излучать электромагнитные волны и вследствие этого непрерывно терять энергию. В результате электроны будут приближаться к ядру и в конце концов упадут на него. Таким образом, атом Резерфорда оказывается неустойчивой системой, что опять-таки противоречит действительности.
Попытки построить модель атома в рамках классической физики не привели к успеху: модель Томсона была опровергнута опытами Резерфорда, ядерная же модель оказалась неустойчивой электродинамически и противоречила опытным данным. Преодоление возникших трудностей потребовало создания качественно новой – квантовой – теории атома.
В 1914 году началась первая мировая война и Резерфорду пришлось на время отложить свои исследования. Но периодически, работая на военную промышленность, он возвращался к своим собственным экспериментам. В своих следующих экспериментах Резерфорд планировал взломать атом.
Эти попытки увенчались полным и потрясающим успехом. Новый взлет Резерфордовского гения привел к открытию, которое впоследствии революционизировало всю науку и технику современности. Был дан первый сигнал к началу атомного века. Резерфорд расщепил атомное ядро.
Мысль об этом возникла у Резерфорда при наблюдении в камере Вильсона (к тому времени она была уже изобретена и усовершенствована) и в стинцилляционном счетчике загадочных треков (следов), гораздо более длинных, чем треки;-частиц, хорошо знакомых ему по бесчисленным опытам. Он подумал, что существуют какие-то неизвестные ему причины резкого удлинения пробега;-частиц. Другое предположение (оно оказалось правильным) заключается в том, что длинные следы оставляют другие неопознанные частицы. Перед исследователем возникла задача выяснить, какое из двух предположений истинно.
Для получения ответа на свои вопросы Резерфорд решил выполнить серию опытов по бомбардировке;-частицами различных веществ. Он построил прибор, который нам кажется теперь необыкновенно простым. Но мы должны признать также, что только он был наиболее пригоден для наглядного решения задачи. В нем мишенями для бомбардировки должны были быть газы (т.е. легкие атомы), а не металлические пластинки, обычно использовавшиеся Резерфордом во многих предыдущих опытах.
Собственно построенный Резерфордом прибор, с помощью которого ему удалось впервые расщепить ядра атомов легких элементов, схематически изображен на рисунке.
Латунная трубка 6 длин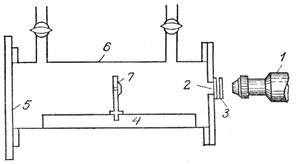 ой 20 см с двумя кранами наполняется газом. Внутри трубки находится диск радиоактивного излучателя 7, испускающего;-частицы. Диск этот укреплен на стойке, двигающейся по рельсу 4. Во время опыта один конец трубки закрывается матовой стеклянной пластинкой, а другой конец – стеклянной пластинкой (прикрепляемой воском). Маленькое прямоугольное отверстие в латунной пластинке закрывалось серебряной пластинкой 3. Серебряная пластинка обладала способностью задерживать;-частицы, эквивалентные слою воздуха толщиной примерно 5 см. Против отверстия помещался люминесцирующий экран из цинковой обманки. Для счета сцинтилляций исследователь пользовался зрительной трубой 1.
ой 20 см с двумя кранами наполняется газом. Внутри трубки находится диск радиоактивного излучателя 7, испускающего;-частицы. Диск этот укреплен на стойке, двигающейся по рельсу 4. Во время опыта один конец трубки закрывается матовой стеклянной пластинкой, а другой конец – стеклянной пластинкой (прикрепляемой воском). Маленькое прямоугольное отверстие в латунной пластинке закрывалось серебряной пластинкой 3. Серебряная пластинка обладала способностью задерживать;-частицы, эквивалентные слою воздуха толщиной примерно 5 см. Против отверстия помещался люминесцирующий экран из цинковой обманки. Для счета сцинтилляций исследователь пользовался зрительной трубой 1.
Когда Резерфорд наполнил трубку азотом, то в поле зрения появились частицы, оставляющие очень длинный след, подобно тому, что он уже наблюдал. Конечно, Резерфорд, прежде чем прийти к окончательным выводам, проделал еще много опытов. Но окончательное заключение было таково: при столкновении;-частиц с ядрами азота, некоторые из этих ядер разрушаются, испуская ядра водорода – протоны, а затем происходит образование ядра кислорода.
Колоссальное значение этого открытия было с самого начала ясно самому Резерфорду и его сотрудникам. Впервые осуществилось расщепление атомных ядер. Непоколебимые, как казалось до этого, представления о «неразложимости» химических элементов были наглядно опровергнуты. Открывались совершенно новые и удивительные возможности искусственного получения одних элементов из других, выделения огромной энергии, содержащейся в ядрах, и т.д.
Продолжая исследования, он получает экспериментальное подтверждение ранее уже установленного им положения – что небольшое количество атомов азота при бомбардировке распадается, испуская быстрые протоны – ядра водорода. В свете позднейших исследований, писал Резерфорд, «общий механизм этого превращения вполне ясен. Время от времени;-частицы действительно проникают в ядро азота, образуя на мгновение новое ядро типа ядра фтора с массой 18 и зарядом 9. Это ядро, которое в природе не существует, чрезвычайно неустойчиво и сразу же распадается, выбрасывая протон и превращаясь в устойчивое ядро кислорода с массой 17 …»
В результате длительных экспериментов Резерфорду удалось вызвать ядерные реакции в 17 легких элементах.
Продолжая опыты по расщеплению ядер, Резерфорд пришел к следующему выводу: хотя;-частицы и обладают большой энергией, но для проникновения в ядра элементов они все же являются недостаточно мощными снарядами. Он решил повысить энергию частиц, разгоняя их в высоковольтной установке. Так был сделан первый шаг в развитии ускорительной техники.
-
Список литературы:
1) Ф.Федоров. «Цепная реакция идеи», изд. «Знание», М., 1975г.
2) Т.И.Трофимова. «Курс физики», изд. «Высшая школа», М., 1999г.
3) «Курс общей физики», Г.А.Зисман, О.М.Тодес, изд. «Эдельвейс», Киев, 1994г.
